Iodometano
| Iodometano | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| iodometano | |
| Nomi alternativi | |
| ioduro di metile | |
| Caratteristiche generali | |
| Formula bruta o molecolare | CH3I |
| Massa molecolare (u) | 141,94 |
| Aspetto | liquido incolore dall'odore acre |
| Numero CAS | 74-88-4 |
| Numero EINECS | 200-819-5 |
| PubChem | 6328 |
| SMILES | CI |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 2,28 |
| Indice di rifrazione | 1,531 |
| Solubilità in acqua | 14 g/L (20 °C) |
| Temperatura di fusione | −66,5 °C (206,65 K) |
| Temperatura di ebollizione | 42,5 °C (315,65 K) |
| Tensione di vapore (Pa) a 293,15 K | 50.000 |
| Proprietà tossicologiche | |
| DL50 (mg/kg) | 76 (orale, ratto) |
| Indicazioni di sicurezza | |
| Punto di fiamma | −28 °C (245,15 K) |
| Simboli di rischio chimico | |
  | |
| pericolo | |
| Frasi H | 301 - 312 - 315 - 331 - 335 - 351 |
| Consigli P | 261 - 280 - 301+310 - 311 [1] |
| Modifica dati su Wikidata · Manuale | |
Lo iodometano, comunemente chiamato anche ioduro di metile, è un composto chimico ottenuto sostituendo un atomo di idrogeno del metano con uno di iodio. A temperatura ambiente si presenta come un liquido incolore miscibile nei solventi organici. In natura viene emesso in piccole quantità dalle piantagioni di riso.[2] Viene utilizzato nella sintesi organica come agente metilante e ne viene proposto l'utilizzo in agricoltura come agente fumigante in sostituzione del bromometano,[3] bandito dal protocollo di Montréal.
Sintesi
Lo iodometano viene sintetizzato facendo reagire il metanolo con triioduro di fosforo, ottenuto in situ utilizzando iodio e fosforo rosso:[4]
Un metodo di sintesi alternativo sfrutta la reazione tra dimetilsolfato e ioduro di potassio in presenza di carbonato di calcio:[4]
Lo iodometano può essere purificato tramite distillazione e successivo lavaggio con tiosolfato di sodio per rimuovere le tracce di iodio.
Un altro metodo di sintesi utilizza metanolo e ioduro di potassio in presenza di acido solforico:
La reazione viene condotta a bassa temperatura e l'acqua prodotta viene assorbita dall'eccesso di acido solforico, spostando in questo modo l'equilibrio verso destra. Lo iodometano ottenuto può essere distillato dalla miscela di reazione.
Reazioni
Lo iodometano è un eccellente substrato per le reazioni SN2, stericamente poco impedito e con lo iodio che costituisce un buon gruppo uscente. Viene utilizzato per alchilare nucleofili contenenti atomi di carbonio, ossigeno, zolfo, azoto e fosforo.[5] Per esempio può essere utilizzato per la metilazione di fenoli e acidi carbossilici:[6]
Un altro esempio è rappresentato dalla metilazione dell'ammoniaca, con formazione di derivati delle ammine (ioduri di metilammonio):
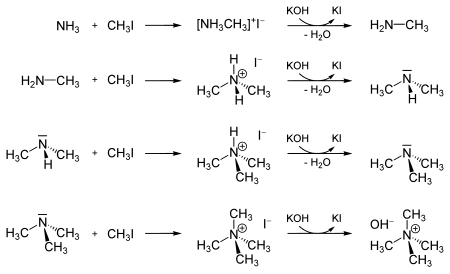
Lo iodometano può essere utilizzato come precursore del reattivo di Grignard CH3MgI, il cui utilizzo è stato alquanto soppiantato dal metillitio commercialmente disponibile.
Nel processo Monsanto, lo ioduro di metile si forma in situ per reazione tra metanolo e acido iodidrico. Successivamente CH3I reagisce con il monossido di carbonio in presenza di un complesso del rodio formando CH3COI (ioduro di acetile), che dopo idrolisi produce acido acetico.
Sicurezza
Tossicità ed effetti biologici
Lo iodometano presenta una tossicità acuta da moderata ad alta per inalazione e ingestione[7]. Il Centers for Disease Control and Prevention (CDC) elenca l'inalazione, l'assorbimento cutaneo, l'ingestione e il contatto con gli occhi come possibili vie di esposizione con gli organi bersaglio degli occhi, della pelle, del sistema respiratorio e del sistema nervoso centrale. I sintomi possono includere irritazione agli occhi, nausea, vomito, vertigini, atassia, linguaggio confuso e dermatite[8]. Nella tossicità acuta ad alte dosi, come può verificarsi in incidenti sul lavoro, la tossicità include disturbi metabolici, insufficienza renale, trombosi venosa e arteriosa ed encefalopatia con convulsioni e coma, con un pattern caratteristico di danno cerebrale[9].
Lo iodometano ha una LD50 per la somministrazione orale ai ratti di 76 mg/kg e nel fegato subisce una rapida conversione in S-metilglutatione.[10] È classificato come potenzialmente cancerogeno da varie agenzie attive nell'ambito medico e ambientale. Lo IARC lo pone all'interno della categoria 3 (classificazione impossibile riguardo all'azione cancerogena per l'uomo).
La sua tossicità deriva dalla sua potente azione metilante: gli enzimi contenenti gruppi solfidrili -SH risentono particolarmente dell'effetto di questo tipo di sostanze, e vengono inibiti. A risentirne in particolare è il sistema nervoso centrale, dove la mancanza di questi enzimi provoca danni gravi.
Note
- ^ Sigma Aldrich; rev. del 13.05.2014
- ^ (EN) K.R. Redeker, N.Y. Wang, J.C. Low, A. McMillan, S.C. Tyler e R.J. Cicerone, Emissions of Methyl Halides and Methane from Rice Paddies, in Science, vol. 290, n. 5493, 2000, pp. 966–969, DOI:10.1126/science.290.5493.966.
- ^ (EN) Marla Cone, EPA OKs use of toxic pesticide on fields, in Los Angeles Times, 6 ottobre 2007. URL consultato il 4 marzo 2011.
- ^ a b (EN) King, C.S. e Hartman, W.W., Methyl Iodide, in Org. Synth., vol. 2, 5 giugno 2011, p. 399.
- ^ (EN) Sulikowski, Gary A., Sulikowski, Michelle M., Haukaas, Michael H. e Moon, Bongjin, Iodomethane, 15 ottobre 2005, DOI:10.1002/047084289X.ri029m.pub2.
- ^ (EN) Avila-Zárraga, J.G. e Martínez, R., Efficient methylation of carboxylic acids with potassium hydroxide/methyl sulfoxide and iodomethane, in Synthetic Communications, vol. 31, n. 14, gennaio 2001, pp. 2177–2183, DOI:10.1081/SCC-100104469.
- ^ (EN) Mingxin Guo e Suduan Gao, Degradation of Methyl Iodide in Soil: Effects of Environmental Factors (PDF), in Journal of Environmental Quality, vol. 38, n. 2, 2009, pp. 513-519, DOI:10.2134/jeq2008.0124. URL consultato il 7 gennaio 2022 (archiviato dall'url originale il 14 agosto 2011).
- ^ (EN) CDC - NIOSH Pocket Guide to Chemical Hazards - Methyl iodide, su cdc.gov.
- ^ (EN) Ivan Iniesta, Mark Radon e Colin Pinder, Methyl iodide rhombencephalopathy: clinico-radiological features of a preventable, potentially fatal industrial accident, in Practical Neurology, vol. 13, n. 6, 2013, pp. 393–395, DOI:10.1136/practneurol-2013-000565.
- ^ (EN) Johnson, M.K., Metabolism of iodomethane in the rat, in Biochem. J., vol. 98, n. 1, gennaio 1966, pp. 38–43, DOI:10.1042/bj0980038.
Altri progetti
Altri progetti
- Wikimedia Commons
 Wikimedia Commons contiene immagini o altri file su iodometano
Wikimedia Commons contiene immagini o altri file su iodometano
V · D · M | |
|---|---|
| Monosostituiti | CH3F · CH3Cl · CH3Br · CH3I |
| Disostituiti | CH2F2 · CH2ClF · CH2BrF · CH2FI · CH2Cl2 · CH2BrCl · CH2ClI · CH2Br2 · CH2BrI · CH2I2 |
| Trisostituiti | CHF3 · CHClF2 · CHBrF2 · CHF2I · CHCl2F · C*HBrClF · C*HClFI · CHBr2F · C*HBrFI · CHFI2 · CHCl3 · CHBrCl2 · CHCl2I · CHBr2Cl · C*HBrClI · CHClI2 · CHBr3 · CHBr2I · CHBrI2 · CHI3 |
| Tetrasostituiti | CF4 · CClF3 · CBrF3 · CF3I · CCl2F2 · CBrClF2 · CClF2I · CBr2F2 · CBrF2I · CF2I2 · CCl3F · CBrCl2F · CCl2FI · CBr2ClF · C*BrClFI · CClFI2 · CBr3F · CBr2FI · CBrFI2 · CFI3 · CCl4 · CBrCl3 · CCl3I · CBr2Cl2 · CBrCl2I · CCl2I2 · CBr3Cl · CBr2ClI · CBrClI2 · CClI3 · CBr4 · CBr3I · CBr2I2 · CBrI3 · CI4 |
| * Composto chirale | |
V · D · M | |
|---|---|
| Ioduri inorganici | Acido iodidrico · Ioduro d'ammonio · Ioduro d'argento · Ioduro di alluminio · Ioduro di bario · Ioduro di berillio · Ioduro di bismuto · Ioduro di cadmio · Ioduro di calcio · Ioduro di cesio · Ioduro di cobalto(II) · Ioduro di cromo(III) · Ioduro ferroso · Ioduro di gallio(III) · Ioduro d'indio · Ioduro di litio · Ioduro di magnesio · Ioduro di manganese(II) · Ioduro mercurico · Ioduro mercuroso · Ioduro di nichel(II) · Ioduro d'oro · Ioduro di piombo · Ioduro di potassio · Ioduro rameoso · Ioduro di rubidio · Ioduro di samario(II) · Ioduro di sodio · Ioduro di stagno(II) · Ioduro di stagno(IV) · Ioduro di stronzio · Ioduro di tallio · Ioduro di zinco · Ioduro di zirconio · Ioduro di vanadio(IV) · Tetraioduro di difosforo · Tetraioduro di silicio · Tetraioduro di tellurio · Tetraioduro di titanio · Tetraioduro d'uranio · Triioduro di antimonio · Triioduro di arsenico · Triioduro di boro · Triioduro di fosforo · Triioduro di tallio · Triioduro d'uranio |
| Organoioduri | Acido acetrizoico · Acido diatrizoico · Acido iocarmico · Adosterolo · Amiodarone · Difenileneiodonio cloruro · Diiodometano · Esaiodobenzene · Iodobenzene · Iodoformio · Iodometano · Ioduro di acetile · Tetraiodometano |
| Controllo di autorità | LCCN (EN) sh2011000498 · GND (DE) 4298750-7 · J9U (EN, HE) 987007590603505171 |
|---|
 Portale Chimica: il portale della scienza della composizione, delle proprietà e delle trasformazioni della materia
Portale Chimica: il portale della scienza della composizione, delle proprietà e delle trasformazioni della materia















 Iodometano
Iodometano