| COL5A1 |
|---|
 |
| Наявні структури |
|---|
| PDB | Пошук ортологів: PDBe RCSB |
|---|
| Список кодів PDB | | 1A89, 1A9A | | |
| Ідентифікатори |
|---|
| Символи | COL5A1, EDSC, collagen type V alpha 1, collagen type V alpha 1 chain, EDSCL1, FMDMF |
|---|
| Зовнішні ІД | OMIM: 120215 MGI: 88457 HomoloGene: 55434 GeneCards: COL5A1 |
|---|
| |
| Пов'язані генетичні захворювання |
|---|
| type I Ehlers-Danlos syndrome[1] |
| |
| Реагує на сполуку |
|---|
| ocriplasmin[2] |
| Онтологія гена |
|---|
| Молекулярна функція | • extracellular matrix structural constituent
• зв'язування з іоном металу
• integrin binding
• platelet-derived growth factor binding
• proteoglycan binding
• heparin binding
• GO:0001948, GO:0016582 protein binding
• extracellular matrix structural constituent conferring tensile strength
|
|---|
| Клітинна компонента | • колаген
• endoplasmic reticulum lumen
• collagen type V trimer
• базальна мембрана
• екзосома
• GO:0005578 Позаклітинна матриця
• міжклітинний простір
• extracellular region
• collagen-containing extracellular matrix
|
|---|
| Біологічний процес | • eye morphogenesis
• negative regulation of endodermal cell differentiation
• tendon development
• wound healing, spreading of epidermal cells
• integrin biosynthetic process
• heart morphogenesis
• regulation of cellular component organization
• extracellular matrix organization
• адгезія клітин
• blood vessel development
• collagen biosynthetic process
• collagen catabolic process
• cell migration
• skin development
• collagen fibril organization
• supramolecular fiber organization
|
|---|
| Джерела:Amigo / QuickGO | |
| Шаблон експресії |
|---|

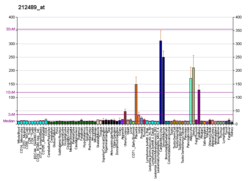
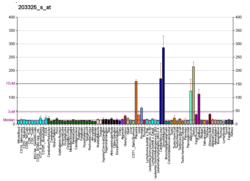 |
| Більше даних |
| Ортологи |
|---|
| Види | Людина | Миша |
|---|
| Entrez | | |
|---|
| Ensembl | | |
|---|
| UniProt | | |
|---|
| RefSeq (мРНК) | | |
|---|
| RefSeq (білок) | | |
|---|
| Локус (UCSC) | Хр. 9: 134.64 – 134.84 Mb | Хр. 2: 27.78 – 27.93 Mb |
|---|
| PubMed search | [3] | [4] |
|---|
| Вікідані |
| Див./Ред. для людей | Див./Ред. для мишей |
|
COL5A1 (англ. Collagen type V alpha 1 chain) – білок, який кодується однойменним геном, розташованим у людей на короткому плечі 9-ї хромосоми.[5] Довжина поліпептидного ланцюга білка становить 1 838 амінокислот, а молекулярна маса — 183 560[6].
Послідовність амінокислот
| 10 | | 20 | | 30 | | 40 | | 50 |
|---|
| MDVHTRWKAR | | SALRPGAPLL | | PPLLLLLLWA | | PPPSRAAQPA | | DLLKVLDFHN |
| LPDGITKTTG | | FCATRRSSKG | | PDVAYRVTKD | | AQLSAPTKQL | | YPASAFPEDF |
| SILTTVKAKK | | GSQAFLVSIY | | NEQGIQQIGL | | ELGRSPVFLY | | EDHTGKPGPE |
| DYPLFRGINL | | SDGKWHRIAL | | SVHKKNVTLI | | LDCKKKTTKF | | LDRSDHPMID |
| INGIIVFGTR | | ILDEEVFEGD | | IQQLLFVSDH | | RAAYDYCEHY | | SPDCDTAVPD |
| TPQSQDPNPD | | EYYTEGDGEG | | ETYYYEYPYY | | EDPEDLGKEP | | TPSKKPVEAA |
| KETTEVPEEL | | TPTPTEAAPM | | PETSEGAGKE | | EDVGIGDYDY | | VPSEDYYTPS |
| PYDDLTYGEG | | EENPDQPTDP | | GAGAEIPTST | | ADTSNSSNPA | | PPPGEGADDL |
| EGEFTEETIR | | NLDENYYDPY | | YDPTSSPSEI | | GPGMPANQDT | | IYEGIGGPRG |
| EKGQKGEPAI | | IEPGMLIEGP | | PGPEGPAGLP | | GPPGTMGPTG | | QVGDPGERGP |
| PGRPGLPGAD | | GLPGPPGTML | | MLPFRFGGGG | | DAGSKGPMVS | | AQESQAQAIL |
| QQARLALRGP | | AGPMGLTGRP | | GPVGPPGSGG | | LKGEPGDVGP | | QGPRGVQGPP |
| GPAGKPGRRG | | RAGSDGARGM | | PGQTGPKGDR | | GFDGLAGLPG | | EKGHRGDPGP |
| SGPPGPPGDD | | GERGDDGEVG | | PRGLPGEPGP | | RGLLGPKGPP | | GPPGPPGVTG |
| MDGQPGPKGN | | VGPQGEPGPP | | GQQGNPGAQG | | LPGPQGAIGP | | PGEKGPLGKP |
| GLPGMPGADG | | PPGHPGKEGP | | PGEKGGQGPP | | GPQGPIGYPG | | PRGVKGADGI |
| RGLKGTKGEK | | GEDGFPGFKG | | DMGIKGDRGE | | IGPPGPRGED | | GPEGPKGRGG |
| PNGDPGPLGP | | PGEKGKLGVP | | GLPGYPGRQG | | PKGSIGFPGF | | PGANGEKGGR |
| GTPGKPGPRG | | QRGPTGPRGE | | RGPRGITGKP | | GPKGNSGGDG | | PAGPPGERGP |
| NGPQGPTGFP | | GPKGPPGPPG | | KDGLPGHPGQ | | RGETGFQGKT | | GPPGPPGVVG |
| PQGPTGETGP | | MGERGHPGPP | | GPPGEQGLPG | | LAGKEGTKGD | | PGPAGLPGKD |
| GPPGLRGFPG | | DRGLPGPVGA | | LGLKGNEGPP | | GPPGPAGSPG | | ERGPAGAAGP |
| IGIPGRPGPQ | | GPPGPAGEKG | | APGEKGPQGP | | AGRDGLQGPV | | GLPGPAGPVG |
| PPGEDGDKGE | | IGEPGQKGSK | | GDKGEQGPPG | | PTGPQGPIGQ | | PGPSGADGEP |
| GPRGQQGLFG | | QKGDEGPRGF | | PGPPGPVGLQ | | GLPGPPGEKG | | ETGDVGQMGP |
| PGPPGPRGPS | | GAPGADGPQG | | PPGGIGNPGA | | VGEKGEPGEA | | GEPGLPGEGG |
| PPGPKGERGE | | KGESGPSGAA | | GPPGPKGPPG | | DDGPKGSPGP | | VGFPGDPGPP |
| GEPGPAGQDG | | PPGDKGDDGE | | PGQTGSPGPT | | GEPGPSGPPG | | KRGPPGPAGP |
| EGRQGEKGAK | | GEAGLEGPPG | | KTGPIGPQGA | | PGKPGPDGLR | | GIPGPVGEQG |
| LPGSPGPDGP | | PGPMGPPGLP | | GLKGDSGPKG | | EKGHPGLIGL | | IGPPGEQGEK |
| GDRGLPGPQG | | SSGPKGEQGI | | TGPSGPIGPP | | GPPGLPGPPG | | PKGAKGSSGP |
| TGPKGEAGHP | | GPPGPPGPPG | | EVIQPLPIQA | | SRTRRNIDAS | | QLLDDGNGEN |
| YVDYADGMEE | | IFGSLNSLKL | | EIEQMKRPLG | | TQQNPARTCK | | DLQLCHPDFP |
| DGEYWVDPNQ | | GCSRDSFKVY | | CNFTAGGSTC | | VFPDKKSEGA | | RITSWPKENP |
| GSWFSEFKRG | | KLLSYVDAEG | | NPVGVVQMTF | | LRLLSASAHQ | | NVTYHCYQSV |
| AWQDAATGSY | | DKALRFLGSN | | DEEMSYDNNP | | YIRALVDGCA | | TKKGYQKTVL |
| EIDTPKVEQV | | PIVDIMFNDF | | GEASQKFGFE | | VGPACFMG |
Білок має сайт для зв'язування з іонами металів, іоном кальцію, з молекулою гепарину. Локалізований у позаклітинному матриксі. Також секретований назовні.
Література
- Seyer J.M., Kang A.H. (1989). Covalent structure of collagen: amino acid sequence of three cyanogen bromide-derived peptides from human alpha 1(V) collagen chain. Arch. Biochem. Biophys. 271: 120—129. PMID 2496661 DOI:10.1016/0003-9861(89)90262-2
- Tillet E., Ruggiero F., Nishiyama A., Stallcup W.B. (1997). The membrane-spanning proteoglycan NG2 binds to collagens V and VI through the central nonglobular domain of its core protein. J. Biol. Chem. 272: 10769—10776. PMID 9099729 DOI:10.1074/jbc.272.16.10769
- Giunta C., Steinmann B. (2000). Compound heterozygosity for a disease-causing G1489E and disease-modifying G530S substitution in COL5A1 of a patient with the classical type of Ehlers-Danlos syndrome: an explanation of intrafamilial variability?. Am. J. Med. Genet. 90: 72—79. PMID 10602121 DOI:10.1002/(SICI)1096-8628(20000103)90:1<72::AID-AJMG13>3.0.CO;2-C
- Greenspan D.S., Cheng W., Hoffman G.G. (1991). The pro-alpha-1(V) collagen chain: complete primary structure, distribution of expression, and comparison with the pro-alpha-1(XI) collagen chain. J. Biol. Chem. 266: 24727—24733. PMID 1722213
- Mann K. (1992). Isolation of the alpha 3-chain of human type V collagen and characterization by partial sequencing. Biol. Chem. Hoppe-Seyler. 373: 69—75. PMID 1571108
- de Paepe A., Nuytinck L., Hausser I., Anton-Lamprecht I., Naeyaert J.-M. (1997). Mutations in the COL5A1 gene are causal in the Ehlers-Danlos syndromes I and II. Am. J. Hum. Genet. 60: 547—554. PMID 9042913
Примітки
- ↑ Захворювання, генетично пов'язані з COL5A1 переглянути/редагувати посилання на ВікіДаних.
- ↑ Сполуки, які фізично взаємодіють з COL5A1 переглянути/редагувати посилання на ВікіДаних.
- ↑ Human PubMed Reference:.
- ↑ Mouse PubMed Reference:.
- ↑ HUGO Gene Nomenclature Commitee, HGNC:2209 (англ.) . Архів оригіналу за 10 вересня 2015. Процитовано 8 вересня 2017.
- ↑ UniProt, P20908 (англ.) . Архів оригіналу за 2 листопада 2017. Процитовано 8 вересня 2017.
Див. також
 Портал «Біологія» Портал «Біологія»  Портал «Хімія» Портал «Хімія»
|
 | Це незавершена стаття про білки.
Ви можете допомогти проєкту, виправивши або дописавши її. |















 COL5A1
COL5A1